O que toda gestante precisa saber e fazer sobre descolamento prematuro da placenta?
Glaucius Nascimento em 1 de janeiro de 2021
- O descolamento prematuro da placenta conceitua-se como a separação da placenta da parede uterina, levando muitas vezes a algum grau de sangramento genital, geralmente no terceiro trimestre.
- Este sangramento pode ser leve ou discreto, moderado e acentuado.
- Um sangramento leve mancha o absorvente (ou a vestimenta íntima) enquanto o grave, preenche todo o absorvente.
- O descolamento oculto da placenta, quando não há nenhum tipo de sangramento é caracterizado por dores no local da implantação placentária, que muitas vezes pode confundir com dores epigátricas e hipocôndrio direito e esquerdo, apresentando como diagnósticos diferenciais gastrite, colecistite e litíase urinária.
- Pacientes portadoras das formas mais graves de sangramento (moderado e intenso) devem se comunicar imediatamente ao médico obstetra assistente e procurar imediatamente uma maternidade. Não se deve esperar pelo médico assistente, ao contrário deve-se agilizar o parto.
- Na suspeita de DPP, considera-se o conduta que é ultimar o parto
- Em relação ao tipo de parto, há uma chance muito maior de o porto ser uma cesariana de emergência e quando a equipe médica e de enfermagem agem de maneira rápida e eficiente os resultados maternos e perinatais são melhores
- Parto normal pode ser realizado se a previsão do parto ocorrer em torno de 20 minutos
- A ultrassonografia pouco ajuda, pode atrapalhar: o diagnóstico é iminentemente clínico
- Não existe clampeamento tardio do cordão no DPP, a cesariana deve ser realizada de maneira ágil para que o sangramento periparto seja minimizado, bem como a necessidade de hemotransfusão
- Alguns casos podem evoluir com óbito fetal, necessidade de hemotransfusão, histerectomia e distúrbio de coagulação, daí porque a sensibilização pela procura rápida pelo serviço de saúde, bem como pela agilidade das pelos profissionais de saúde
- Nos casos de DPP com distúrbio de coagulação, vale a pena no momento oportuno a investigação de trombofilia
- Há 10 anos, minha esposa teve um quadro de DPP oculto, morte fetal e distúrbio de coagulação (CIVD) com necessidade de inúmeras transfusões. Perdi meu filho Mateus para um DPP oculto, mas não desisti de continuar lutando. Posteriormente descobrimos que ela é portadora de trombofilia. Depois do DPP, engravidou duas vezes e hoje sou pai de Allana, João Pedro e Miguel. Valeu a pena demais, não sinto mais nenhuma dor e hoje ajudo inúmeros casais a realizarem o sonho da maternidade, principalmente aqueles que passaram por desfechos maternos e perinatais negativos.
- Há dois dias, numa cesariana de emergência, uma paciente minha apresentou DPP grave e graças a Deus e a uma equipe médica e de enfermagem célere, não tivemos nenhum desfecho materno ou perinatal negativo.
Alguma imagens sobre Descolamento Prematuro da Placenta
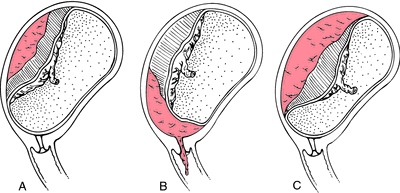
Fonte: https://medical-dictionary.thefreedictionary.com/premature+separation+of+the+placenta
Figura A demonstrando um DPP moderado oculto
Figura B demonstrando um DPP leve com sangramento genital
Figura C demonstrando um DPP grave oculto
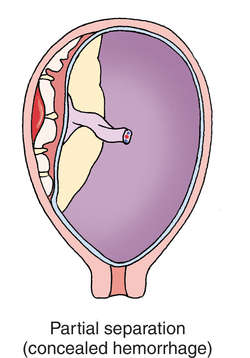

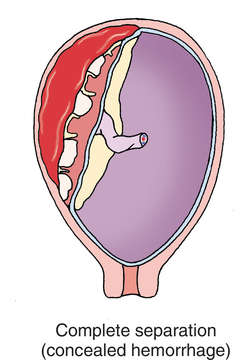
Fonte: https://medical-dictionary.thefreedictionary.com/premature+separation+of+the+placenta
Da esquerda pra direita, imagem 1 evidencia separação parcial da placenta com a parede uterina, leve e oculta (DPP leve oculto); imagem 2 um DPP com sangramento leve a moderado e a imagem 3 um DPP oculto grave com sepração total da massa placentária da parede uterina.

Fonte: https://slideplayer.com.br/slide/10368981/
Macroscopia de um hematoma retroplacentário

Fonte: https://radiopaedia.org/cases/placental-abruption
Imagem ultrassonográfica de um hematoma retroplacentário
Descolamento Prematuro da Placenta – Protocolo FEBRASGO
Feitosa FE, Carvalho FH, Feitosa IS, Paiva JP. Descolamento prematuro de placenta. São Paulo: Federação Brasileira das Associações de Ginecologia e Obstetrícia (FEBRASGO); 2018. (Protocolo FEBRASGO – Obstetrícia, no. 27/ Comissão Nacional Especializada em Urgências Obstétricas).
Introdução
O descolamento prematuro de placenta (DPP) é a separação da placenta normalmente inserida, de forma parcial ou completa, antes do nascimento do feto. O diagnóstico, geralmente, é reservado para gestações com 20 ou mais semanas. Os achados clínicos principais são sangramento vaginal e dor abdominal, muitas vezes, acompanhados por contrações uterinas hipertônicas e um padrão de frequência cardíaca fetal não tranquilizador. (1-4) Representa causa significativa de morbi-mortalidade materna e perinatal. A taxa de mortalidade perinatal é aproximadamente 20 vezes maior em
relação às gestações sem DPP (12% versus 0,6%, respectivamente).
A maioria das mortes perinatais (até 77%) ocorre intraútero. É a prematuridade a principal causa de mortalidade pós-natal. (5)
Classificação
É classificado em três graus, levando-se em conta os achados clínicos e laboratoriais:(4,5)
• Grau I: Assintomático ou apresenta sangramento genital discreto, sem hipertonia uterina significativa e com vitalidade
fetal preservada. Sem repercussões hemodinâmicas e coagulopatias materna. O diagnóstico é realizado após o nascimento
por presença de coágulo retroplacentário.
• Grau II: Sangramento genital moderado com hipertonia uterina. Repercussões hemodinâmicas na mãe, com aumento de frequência cardíaca, alterações posturais da pressão arterial e queda do nível de fibrinogênio. Feto vivo, porém com vitalidade fetal prejudicada.
• Grau III: Caracteriza-se por óbito fetal e alterações mais acentuadas de hipotensão arterial materna e hipertonia uterina.
Divide-se em:
– IIIA: Com coagulopatia instalada.
– IIIB: Sem coagulopatia instalada.
Incidência
O DPP complica aproximadamente 1% das gestações, com dois terços classificados como graves devido à mortalidade materna, fetal e neonatal que gera. É responsável por cerca de 10% dos partos prematuros. (4,5) Revisão publicada em 2017 cita que 40% a 60% dos DPPs ocorreram antes das 37 semanas de gestação e 14% ocorreram antes das 32 semanas. No entanto as taxas de incidência de idade gestacional variaram consideravelmente dependendo da etiologia.(5)
Fisiopatologia
A causa imediata do DPP é a ruptura dos vasos maternos na decídua basal. O sangue acumulado atinge a zona de clivagem decíduo-placentária e inicia a separação. O sangramento pode ser pequeno e autolimitado, ou pode continuar a dissecar através da interface placenta-decidual, levando à separação completa ou quase completa da placenta. A porção descolada da placenta é incapaz de permutar gases e nutrientes; quando a unidade fetoplacentária restante é incapaz de compensar essa perda de função, o feto é comprometido. (6,7) A etiologia do sangramento na decídua basal continua a ser especulativa na maioria dos casos, apesar da extensa pesquisa clínica e epidemiológica. Uma pequena proporção dos descolamentos está relacionada a eventos mecânicos súbitos, como traumatismo abdominal ou descompressão uterina rápida, que causam a tração da placenta inelástica devido ao alongamento ou à contração súbita da parede uterina subjacente. Em acidentes automobilísticos, por exemplo, um fator adicional é a rápida aceleração-desaceleração do útero, que causa alongamento uterino sem alongamento placentário concomitante. Embora um trauma menor possa estar associado a um risco aumentado de parto prematuro, o trauma materno grave está associado a um aumento em seis vezes do risco de
descolamento. (5-14) As anormalidades uterinas, o uso de cocaína e o tabagismo são causas menos comuns de DPP. As anomalias uterinas (por exemplo, o útero bicorno), sinéquias uterinas e leiomioma são locais impróprios mecânica e biologicamente para implantação placentária. O descolamento nesses locais pode ser devido a uma decidualização inadequada. O implante trofoblástico subótimo, também, pode explicar o aumento do risco de descolamento entre mulheres com cesariana anterior (odds ratio [OR] 2,3, IC 95% 1,5-3,6).(5-9) O efeito fisiopatológico da cocaína na gênese do DPP é desconhecido, mas pode estar relacionado à vasoconstrição induzida por cocaína, causando isquemia, vasodilatação reflexa e comprometimento da integridade vascular. Cerca de 10% das mulheres que usam cocaína no terceiro trimestre desenvolverão DPP. O mecanismo que está subjacente à relação tabagismo e DPP não está claro. Uma hipótese é que os efeitos vasoconstritores do tabagismo causem hipoperfusão placentária, o que pode resultar em isquemia,
necrose e hemorragia, levando à DPP prematura.(9-11,15) A maioria dos descolamentos parece estar relacionada a um processo patológico placentário crônico. Nesses casos, anormalidades no desenvolvimento precoce das artérias espiraladas provocariam necrose decidual, inflamação placentária e, possivelmente, infarto e, finalmente, disrupção vascular e sangramento.(5,8,10,11) A hemorragia arterial de alta pressão na área central da placenta leva ao desenvolvimento rápido de manifestações clínicas potencialmente fatais de descolamento (por exemplo, sangramento grave, coagulação intravascular disseminada materna e anormalidades da frequência cardíaca fetal). A hemorragia venosa de baixa pressão, tipicamente na periferia da placenta (descolamento marginal), é mais provável que resulte em manifestações clínicas que ocorrem ao longo do tempo (por exemplo, hemorragia intermitente leve, oligo-hidrâmnia e restrição de crescimento fetal associada à redistribuição do fluxo sanguíneo cerebral).(11,16,17) A trombina desempenha um papel fundamental nas consequências clínicas do DPP e também pode ser importante em sua patogênese, sendo formada por duas vias: em um caminho, o sangramento decidual leva à liberação do fator tecidual (tromboplastina) das células deciduais, o que gera trombina. No outro caminho, a hipóxia decorrente induz produção de fator de crescimento endotelial vascular (VEGF), que atua diretamente em células endoteliais deciduais para causar expressão aberrante do fator tecidual, que então gera trombina. A produção de trombina pode levar à hipertonia uterina, produção de fatores inflamatórios capazes de promover rotura prematura das membranas, distúrbio de coagulação e deficiência da ação da progesterona resultando no desencadeamento da atividade uterina.(5,10,11,18,19)
Fatores de risco
O DPP prévio é o fator de risco mais importante para o descolamento, com riscos de recorrência de 10 a 15 vezes maiores
(5) e até 93 vezes mais (95% IC 62-139).(11) As síndromes hipertensivas representam a condição clínica mais frequentemente associada ao DPP. As mulheres hipertensas têm um risco cinco vezes maior de DPP grave em comparação com mulheres normotensas, e a terapia anti-hipertensiva não parece reduzir o risco de descolamento placentário entre mulheres com hipertensão crônica.(5,11) O tabagismo é um dos poucos fatores de risco modificáveis e está associado a um risco aumentado de 2,5 vezes de descolamento suficientemente grave para resultar em morte fetal, sendo que o risco aumenta em 40% para cada maço de cigarro fumado por dia.(16) A combinação de tabagismo e hipertensão tem um efeito sinérgico sobre o risco de descolamento (Quadro 1).
Quadro 1. Fatores de risco
» Sociodemográficos e comportamentais
· Idade materna ≥ 35 anos e < 20 anos
· Paridade ≥ 3
· Raça Negra
· Mães solteiras
· Tabagismo, uso de álcool e drogas
· Infertilidade de causa indeterminada
» Fatores maternos na gestação atual
· Síndromes hipertensivas – responsável por até 50% dos casos de DPP não traumáticos
· Hiper-homocisteinemia
· Trombofilia
· Diabetes pré-gestacional
· Hipotireoidismo
· Anemia
· Mal formação uterina
· Rotura Prematura de Membranas
· Corioamnionite
· Oligoâmnio/Polidrâmnio
· Placenta prévia
· Gestações múltiplas
· Trauma (automobilístico, brevidade do cordão, versão externa, torção do útero
gravídico, retração uterina intensa)
· Amniocentese/Cordocentese
» Fatores maternos em gestações anteriores
· Cesárea anterior
· Abortamentos
· Pré-eclâmpsia
· Natimorto
· Descolamento Prematuro de Placenta – aumenta o risco em 3% a 15 %.
Fonte: Traduzida de Tikkanen M. Placental abruption: epidemiology, risk factors and consequences. Acta Obstet Gynecol Scand. 2011;90(2):140–9.(11)
Um aumento modesto no risco de descolamento também foi observado em mulheres com asma (OR ajustada 1,22, IC 95%
1,09-1,36). (5,11) As irmãs das mulheres que tiveram um DPP parecem apresentar maior risco de ter quadro semelhante (odds ratio de 1,7 a 2,1). (5)
Diagnóstico
O diagnóstico é eminentemente clínico, mas os achados de estudos de imagem, laboratório e pós-parto podem ser utilizados para apoiar o diagnóstico clínico. Mulheres com DPP agudo, classicamente, apresentam-se com sangramento vaginal leve a moderado e dor abdominal e/ou dor nas costas, acompanhadas de contrações uterinas. Em pacientes com sintomas clássicos, anormalidades da frequência cardíaca fetal ou ausência de batimentos e/ou coagulação intravascular disseminada apoiam fortemente o diagnóstico clínico e indicam DPP extenso.(6) O exame de ultrassonografia é útil para identificar um hematoma retroplacentário e para excluir outros distúrbios associados a sangramento vaginal e dor abdominal. Um hematoma retroplacentário é o achado clássico e apoia fortemente o diagnóstico clínico, mas está ausente em muitos pacientes.(6,10,17) Conquanto os piores resultados pareçam ocorrer quando há evidência ecográfica de um hematoma retroplacentário, a ausência de hematoma não exclui a possibilidade de descolamento grave porque ele pode ainda não ter se organizado. A sensibilidade dos achados para o diagnóstico é de apenas 25% a 60%, mas o valor preditivo positivo é alto (88%), quando estão presentes.(6,10,17) No pós-parto, a ausência de achados placentários característicos não exclui o diagnóstico. Num estudo multicêntrico, a avaliação normal e histopatológica da placenta só conseguiu confirmar o diagnóstico clínico em 30% dos casos (49/162).(5,6,11) Achados laboratoriais – O grau de hemorragia materna correlaciona-se com o grau de anormalidade hematológica; os níveis de fibrinogênio apresentam a melhor correlação com a gravidade do sangramento, a coagulação intravascular disseminada e a necessidade de transfusão de múltiplos produtos sanguíneos. Os valores iniciais de fibrinogênio de ≤200 mg/dL têm um valor preditivo positivo de 100% para hemorragia pós-parto grave, enquanto que níveis de ≥400 mg/dL têm um valor preditivo negativo de 79%.(5,6,11,20-24) O DPP leve pode não estar associado a quaisquer anormalidades dos testes de hemostasia comumente usados.(21) O DPP grave pode levar à coagulação intravascular disseminada (CIVD) e, em 10% a 20% desses leva ao óbito fetal.(21) O diagnóstico de CIVD aguda é confirmado pela demonstração de aumento da geração de trombina (por exemplo, diminuição do fibrinogênio) e aumento da fibrinólise (por exemplo, produtos elevados de degradação de fibrina [PDF] e D-dímero). Todavia os achados de laboratório sugestivos de CIVD leve precisam ser interpretados com cautela durante a gravidez devido aos aumentos normais relacionados à concentração de quase todos os fatores de coagulação e uma diminuição
leve normal na contagem de plaquetas que ocorrem fisiologicamente na gestação. (20)
Diagnóstico diferencial
Em mulheres grávidas com suspeita de descolamento, o diagnóstico diferencial de sangramento vaginal, acompanhado de dor e contrações, inclui trabalho de parto, placenta prévia, ruptura uterina e hematoma subcoriônico. Os sinais e sintomas do trabalho têm um início mais gradual do que os de descolamento. O início do trabalho (pré-termo ou termo) é caracterizado por contrações uterinas leves em intervalos infrequentes e/ou irregulares; as contrações tornam-se mais regulares e dolorosas ao longo do tempo e são acompanhadas por dilatação cervical e/ou apagamento. O muco que se acumulou no colo do útero pode ser eliminado como secreção clara, rosa ou ligeiramente sangrenta, às vezes, vários dias antes do início do parto. (5,11) A apresentação clínica característica da placenta prévia é sangramento vaginal indolor após 20 semanas de gestação, no entanto 10% a 20% das mulheres apresentam contrações uterinas associadas ao sangramento. Assim, o DPP e a placenta prévia podem ser difíceis de distinguir clinicamente, uma vez que o descolamento pode não estar associado à dor significativa; e, por sua vez, a placenta prévia pode não ser indolor. Em mulheres grávidas com hemorragia vaginal, uma ultrassonografia deve ser realizada para determinar se a placenta prévia é a fonte do sangramento. (6) A ruptura uterina é mais comum em mulheres com histerotomia prévia. Os sinais de ruptura uterina podem incluir anormalidades do ritmo cardíaco fetal, sangramento vaginal, dor abdominal constante, cessação das contrações uterinas, hipotensão materna e taquicardia. Muitos desses sintomas são comuns ao descolamento porque a ruptura uterina geralmente leva à DPP. (5)
Conduta
A conduta deve ser individualizada e depende da extensão e classificação do DPP, do comprometimento materno e fetal e da idade gestacional (Figura 1).
As gestantes com suspeita de DPP devem ser monitoradas avaliando-se o estado hemodinâmico materno (PA, pulso e diurese) e a vitalidade fetal.(4,6) A avaliação laboratorial materna deve incluir tipagem sanguínea, hemograma completo e coagulograma. Um teste simples, de baixo custo e com resultado rápido pode ser realizado para avaliar o estado de coagulação da gestante, através da coleta de 10ml de sangue em tubo de ensaio seco que deve ser mantido em temperatura ambiente. Após 7 a 10 minutos, deverá haver a formação de um coágulo firme; se isso não ocorrer, a coagulopatia está instalada. A ultrassonografia pode ser útil nos casos duvidosos, pois o diagnóstico é eminentemente clínico.(25,26) A qualquer sinal de hipotensão ou instabilidade hemodinâmica, deve-se instituir dois acessos venosos calibrosos com infusão de 1000 ml de solução cristaloide, com velocidade de infusão de 500 ml nos primeiros 10 minutos e manutenção com 250 ml/h mantendo-se débito urinário > 30mL/h. A monitorização cardíaca fetal contínua desde que o feto esteja em risco de hipoxemia ou desenvolver acidose. De um modo geral, nos casos de feto viável, quando o parto vaginal não for iminente, a via de parto preferida deve ser a abdominal por cesárea de emergência. Nos casos de feto vivo com cardiotocografia (CTG) categoria III e o parto vaginal for iminente (próximos 20 minutos), pode-se optar pelo parto vaginal espontâneo ou instrumental. Se parto vaginal não for iminente, deve-se indicar a cesárea. Nas situações de feto vivo com CTG categoria II: a via de parto dependerá da idade gestacional, dilatação cervical e se existe instabilidade fetal ou materna. Nos fetos vivos com CTG categoria I: a via de parto dependerá da estabilidade hemodinâmica materna e da idade gestacional. Na presença de feto morto e mãe hemodinamicamente estável, deve-se optar pelo parto vaginal. A amniotomia faz-se necessária para reduzir hemorragia materna e passagem de tromboplastina para a corrente sanguínea da mãe. A ocitocina pode ser administrada se houver necessidade de induzir o parto. O parto deverá ocorrer dentro de 4 a 6 horas e o quadro clínico reavaliado a cada hora.(4,6) Após o parto, a monitorização materna rigorosa impõe-se, principalmente quando se identifica a presença de útero de Couvelaire como achado intraoperatório.
Recorrência
As mulheres com DPP apresentam maior risco de descolamento em uma gravidez subsequente. De 3% a 15% das mulheres têm recorrência, em comparação com uma incidência basal de 0,4% a 1,3% na população em geral. Em um estudo longitudinal de base populacional, o risco de descolamento da placenta em uma gravidez subsequente foi de aproximadamente 6% em mulheres com descolamento em sua primeira gravidez contra 0,06% em mulheres sem DPP.(4,5,9,23) Após dois descolamentos consecutivos, o risco de um terceiro aumenta para 20% a 25%.(22,27) O risco de recorrência é maior após um DPP grave do que após um leve. Quando o quadro é suficientemente grave para levar ao óbito fetal, há uma incidência de 7% de DPP com morte fetal em uma gravidez futura.(4,23)
Descolamento crônico
As gestantes com este quadro apresentam hemorragia leve, crônica, intermitente e manifestações clínicas de doença placentária isquêmica que se desenvolvem ao longo do tempo, como oligo-hidrâmnia, restrição de crescimento fetal e pré-eclâmpsia.(4,5,11) Elas também correm o risco de ruptura prematura das membranas. Os estudos de coagulação, comumente, são normais. O exame ultrassonográfico pode identificar hematoma placentário (retromembranoso, marginal ou central), e o exame seriado pode revelar restrição de crescimento fetal e/ou oligo-hidrâmnia. O DPP, no segundo trimestre acompanhado de oligo-hidrâmnia, tem um prognóstico sombrio, incluindo altas taxas de morte fetal, parto prematuro e morbidade neonatal grave ou morte.(4,5,11,27,28) O exame histológico da placenta pode mostrar lesões crônicas, como deciduite crônica, necrose decidual, villite, vasculopatia decidual, infarto placentário, trombose intervilositária e deposição de hemossiderina.(19)
Referências
1. Cunninghan FG, Leveno JK, Bloom MD, Hauth JC, Gilstrap LC 3rd, Westrom KD. Obstetrical hemorrhage. Cunninghan FG, Leveno JK, Bloom MD, Hauth JC, Gilstrap III LC, Westrom KD., editores. Williams obstetrics. 24th ed. New York: McGraw-Hill; 2014. p. 793–9.
2. Zugaib M, Francisco RP. Descolamento prematuro de placenta. In: Zugaib M, Francisco RP, editores. Obstetrícia. 3a ed. São Paulo: Manole. 2017. p. 713–24.
3. Montenegro CA, Rezende Filho J. Descolamento prematuro da placenta. In: Montenegro CA, Rezende Filho J, editor. Rezende obstetrícia. 13a ed. Rio de Janeiro: Guanabara Koogan; 2017.
4. Guidelines Committee of the Royal College of Obstetricians and Gynaecologists (RCOG). Antepartum haemorrhage. Green Top Guidelines. Marylebone, London: RCOG; 2011. (Green–top Guideline No. 63).
5. Ananth CV, Kinzler WL. Placental abruption: clinical features and diagnosis . Uptodate 2017 [Internet]. [cited 2018 Sep 1]. Available from: https://www.uptodate.com/contents/placental-abruption-pathophysiology-clinical-features-diagnosis-and-consequences 6. Oyelese Y, Ananth CV. Placental abruption: management. Uptodate; 2017. Internet]. [cited 2018 Sep 1]. Available from: https://www.uptodate.com/contents/placentalabruption-management
7. Tikkanen M, Luukkaala T, Gissler M, Ritvanen A, Ylikorkala O, Paavonen J, et al. Decreasing perinatal mortality in placental abruption. Acta Obstet Gynecol Scand. 2013;92(3):298–305.
8. Ananth CV, Keyes KM, Hamilton A, Gissler M, Wu C, Liu S, et al. An international contrast of rates of placental abruption: an age-period-cohort analysis. PLoS One. 2015;10(5):e0125246.
9. Ruiter L, Ravelli AC, de Graaf IM, Mol BW, Pajkrt E. Incidence and recurrence rate of placental abruption: a longitudinal linked national cohort study in the Netherlands. Am J Obstet Gynecol. 2015;213(4):573.e1–8.
10. Ananth CV, Lavery JA, Vintzileos AM, Skupski DW, Varner M, Saade G, et al. Severe placental abruption: clinical definition and associations with maternal complications. Am J Obstet Gynecol. 2016;214(2):272.e1–9.
11. Tikkanen M. Placental abruption: epidemiology, risk factors and consequences. Acta Obstet Gynecol Scand. 2011;90(2):140–9.
12. Melamed N, Aviram A, Silver M, Peled Y, Wiznitzer A, Glezerman M, et al. Pregnancy course and outcome following blunt trauma. J Matern Fetal Neonatal Med. 2012;25(9):1612–7.
13. Cheng HT, Wang YC, Lo HC, Su LT, Lin CH, Sung FC, et al. Trauma during pregnancy: a population-based analysis of maternal outcome. World J Surg. 2012;36(12):2767–75.
14. Bauer CR, Shankaran S, Bada HS, Lester B, Wright LL, Krause-Steinrauf H, et al. The Maternal Lifestyle Study: drug exposure during pregnancy and short-term maternal outcomes. Am J Obstet Gynecol. 2002;186(3):487–95.
15. Mbah AK, Alio AP, Fombo DW, Bruder K, Dagne G, Salihu HM. Association between cocaine abuse in pregnancy and placenta-associated syndromes using propensity score matching approach. Early Hum Dev. 2012;88(6):333–7.
16. Kaminsky LM, Ananth CV, Prasad V, Nath C, Vintzileos AM; New Jersey Placental Abruption Study Investigators. The influence of maternal cigarette smoking on placental pathology in pregnancies complicated by abruption. Am J Obstet Gynecol. 2007;197(3):275.e1–5.
17. Morales-Roselló J, Khalil A, Akhoundova F, Salvi S, Morlando M, Sivanathan J, AlberolaRubio J, Hervas-Marín D, Fornés-Ferrer V, Perales-Marín A, Thilaganathan B. Fetal cerebral and umbilical Doppler in pregnancies complicated by late-onset placental abruption. J Matern Fetal Neonatal Med. 2017;30(11):1320-4.
18. Krikun G, Huang ST, Schatz F, Salafia C, Stocco C, Lockwood CJ. Thrombin activation of endometrial endothelial cells: a possible role in intrauterine growth restriction. Thromb Haemost. 2007;97(2):245–53.
19. Incebiyik A, Uyanikoglu H, Hilali NG, Sak S, Turp AB, Sak ME. Does apoptotic activity have a role in the development of the placental abruption? J Matern Fetal Neonatal Med. 2017;30(23):2871–5.
20. Suzuki S. Clinical significance of preterm singleton pregnancies complicated by placental abruption following preterm premature rupture of membranes compared with those without p-PROM. ISRN Obstet Gynecol. 2012;2012:856971.
21. Thachil J, Toh CH. Disseminated intravascular coagulation in obstetric disorders and its acute haematological management. Blood Rev. 2009;23(4):167–76.
22. Lockwood CJ, Kayisli UA, Stocco C, Murk W, Vatandaslar E, Buchwalder LF, et al. Abruptioninduced preterm delivery is associated with thrombin-mediated functional progesterone withdrawal in decidual cells. Am J Pathol. 2012;181(6):2138–48.
23. Abramovici A, Gandley RE, Clifton RG, Leveno KJ, Myatt L, Wapner RJ, et al.; Eunice Kennedy Shriver National Institute of Child Health Human Development MaternalFetal Medicine Units Network. Prenatal vitamin C and E supplementation in smokers is associated with reduced placental abruption and preterm birth: a secondary analysis.
BJOG. 2015;122(13):1740–7.
24. Mendola P, Laughon SK, Männistö TI, Leishear K, Reddy UM, Chen Z, et al. Obstetric complications among US women with asthma. Am J Obstet Gynecol. 2013;208(2):127. e1–8.
25. Rasmussen S, Irgens LM. Occurrence of placental abruption in relatives. BJOG. 2009;116(5):693–9.
26. Kasai M, Aoki S, Ogawa M, Kurasawa K, Takahashi T, Hirahara F. Prediction of perinatal outcomes based on primary symptoms in women with placental abruption. J Obstet Gynaecol Res. 2015;41(6):850–6.
27. Wang L, Matsunaga S, Mikami Y, Takai Y, Terui K, Seki H. Pre-delivery fibrinogen predicts adverse maternal or neonatal outcomes in patients with placental abruption. J Obstet Gynaecol Res. 2016;42(7):796–802.
28. Shinde GR, Vaswani BP, Patange RP, Laddad MM, Bhosale RB. Diagnostic Performance of Ultrasonography for Detection of Abruption and Its Clinical Correlation and Maternal and Foetal Outcome. J Clin Diagn Res. 2016;10(8):QC04–07.






