DISTÚRBIOS DO LÍQUIDO AMNIÓTICO
Polidramnia
A polidramnia foi originalmente definida como volume de líquido amniótico (LA) acima de 2.000 ml no momento do parto. Litzenberg (1941) descreve: “O aumento moderado do líquido amniótico é comum e de pouca significância clínica, sendo que aumentos excessivos, de 15 a 20cm, oferecem problemas clínicos reais.” Para época, esta definição foi de suma importância, por tratar, essencialmente, das complicações intraparto. O desenvolvimento e a inclusão da ultrassonografia no rastreamento pré-natal possibilitaram o refinamento desse diagnóstico antes da ruptura das membranas, nos casos menos exuberantes, mas não sem provocar controvérsias. A principal delas refere-se ao conceito sonográfico do polidrâmnio, fato que pode justificar as discordâncias nos resultados perinatais, na incidência de cesárea e macrossomia observadas em algumas diferentes séries, particularmente nos casos idiopáticos (Fisk et al., 1994).
A incidência da polidrâmnio varia entre 0,2 e 2,0%, sendo a maioria dos casos classificada como idiopática (50 a 60%) (Aviram et al., 2015). São descritas duas formas clínicas: aguda e crônica. A forma aguda, que representa apenas 1,6% dos casos, é caracterizada por aumento de volume do LA em poucos dias, sendo precoce (antes da 24a. semana) e, geralmente, de prognóstico sombrio (Queenan & Gadow, 1970). A outra forma, a crônica, corresponde à maioria absoluta dos casos, de instalação lenta e progressiva, ocorrendo ao fim do 2o. trimestre e no 3o. trimestre da gestação. As causas do aumento de LA podem ser fetais, maternas ou placentárias (Tabela 33.1) e, consequentemente, o prognóstico perinatal dessas gestações varia em função da causa primária.
Etiologia
A etiologia da polidramnia está sempre relacionada com a alteração do balanço entre a produção e a absorção de LA, e 50 a 60% dos casos não têm causa definida, sendo classificados como idiopáticos. O diabetes materno é descrito como causa primária da polidramnia em 8 a 20% (Fisk et al., 1994), e as malformações fetais estão associadas em 4 a 45% dos casos (Magann et al., 2007). Nas malformações fetais, os mecanismos de reabsorção podem estar prejudicados por compressões intrínsecas (atresia esofágica) ou extrínsecas (hérnia diafragmática), alterações da deglutição (micrognatia) ou, então, por aumento na produção de LA por exsudação anômala através dos tecidos (defeitos do tubo neural). No diabetes, a hiperglicemia materna determina diurese osmótica fetal e a maior concentração de solutos na cavidade amniótica. Nos casos idiopáticos, apesar de o mecanismo fisiopatológico do acúmulo excessivo ser desconhecido, é provável que as membranas tenham papel predominante. Diversos fatores, como endotelina-1 (American College of Obstetricians and Gynecologists [ACOG], 2000), peptídio natriurético cerebral humano (ACOG, 2000), aquaporinas (AQP1, AQP3, AQP8, AQP9) (Bajoria et al., 2003) e fator de crescimento endotelial vascular, estão envolvidos no transporte de água das membranas amnióticas, mas a importância relativa desses fatores na alteração do volume de LA ainda não é conhecida. Mann et al. (2006) demonstraram aumento na expressão de aquaporinas (AQP1) de até 33 vezes nas membranas amnióticas de gestações com polidramnia, provavelmente uma resposta compensatória ao aumento do volume de LA (Bajoria et al., 2003).
Diagnóstico
Clínico
A polidramnia só tem expressão clínica ao exame físico quando alcança o volume de 3 a 4L. O diagnóstico clínico é suspeitado inicialmente a partir da observação da altura do fundo uterino acima do esperado para a idade gestacional, da dificuldade na palpação do feto e da ausculta convencional (estetoscópio de Pinard), e pela consistência cística do útero. O agravamento do quadro é acompanhado de hipertonia uterina, dor abdominal e lombar, edema no andar inferior do abdome e membros inferiores, pele do abdome lisa e brilhante com extensas estrias, varizes de membros inferiores, hemorroidas, metrossístoles e ruptura prematura das membranas (RPM). O trabalho de parto prematuro é extremamente comum, mas somente nas gestações complicadas com diabetes e malformações congênitas o grau de polidramnia irá influenciar o risco dele ocorrer (Fisk et al., 1994).
Ultrassonografia
O conceito mais aceito de polidramnia na ultrassonografia (Figura 33.1) a define como identificação do maior bolsão vertical (MBV), com mais de 8 cm, ou por índice do líquido amniótico (ILA) superior a 18 cm, usando os parâmetros semiquantitativos (veja a descrição dos parâmetros em Oligoidramnia). A polidramnia pode, ainda, ser classificada em leve (ILA: 25 a 29 cm; ou MBV: 8 a 11 cm), moderada (ILA: 30 a 34,9 cm; ou MBV: 12 a 15 cm) ou grave (ILA: 35 cm ou MBV: 16 cm) (Magann et al., 2007). O quadro de polidramnia pode ser facilmente identificável por meio da ressonância magnética (RM) quando esta é usada como método complementar para pesquisas de malformações fetais (Figura 33.2).
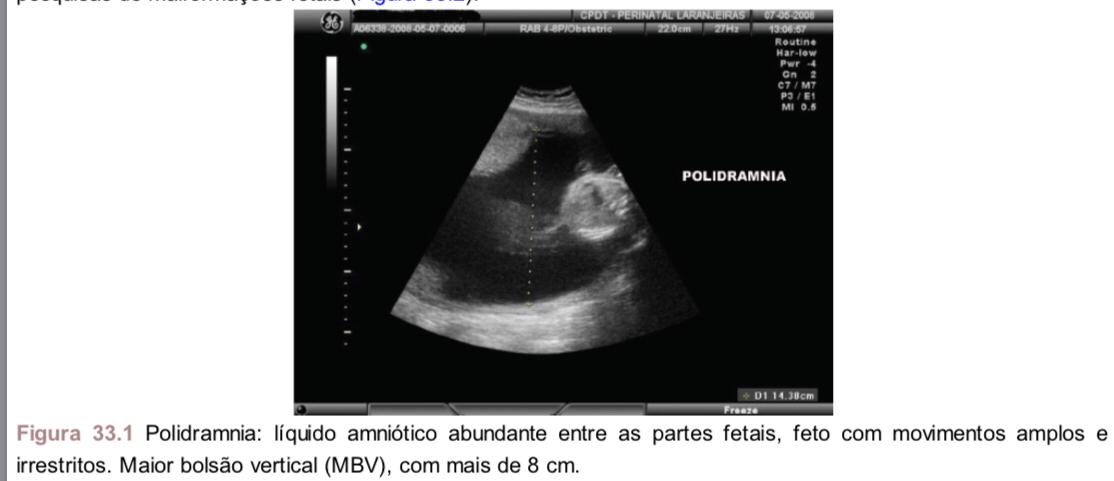 Figura 33.1 Polidramnia: líquido amniótico abundante entre as partes fetais, feto com movimentos amplos e
Figura 33.1 Polidramnia: líquido amniótico abundante entre as partes fetais, feto com movimentos amplos e
irrestritos. Maior bolsão vertical (MBV), com mais de 8 cm.
Na avaliação subjetiva, o diagnóstico depende da percepção do examinador, por meio de movimentos amplos e irrestritos; nos casos mais graves, a placenta pode aparentar espessura reduzida pela distensão da cavidade uterina.
Abordagem diagnóstica
É fundamental a investigação da etiopatogenia, que costuma estar associada a: (1) diabetes materno; (2) infecções congênitas (sífilis, toxoplasmose, citomegalovirose, parvovirose); (3) doença hemolítica perinatal; (4) malformações fetais; e (5) anomalias placentárias. A investigação das malformações pela ultrassonografia (nível II) é de suma importância. O examinador deve estar atento às malformações congênitas mais comumente associadas (Figura 33.3) e às anormalidades placentárias, como a placenta circunvalada e os corioangiomas. As malformações do sistema nervoso central são as mais comumente observadas nos casos de polidramnia (32,4%), seguidas pelas cardíacas (25,9%) e as do sistema gastrintestinal (16,8%) (Magann et al., 2007). Quanto maior o grau de polidramnia, maior a prevalência das malformações fetais, que pode variar de 8% (nas leves) a 31% (nas graves). Quando a polidramnia cursa com o crescimento intrauterino restrito (CIUR), a investigação ultrassonográfica torna-se imperiosa em função do aumento significativo da mortalidade perinatal (OR: 20,6; IC95: 12,6 a 33,4) e neonatal (OR: 29,7; IC95: 16,2 a 54,5), além da morbidade neonatal (OR: 2,7; IC95: 1,2 a 4,1). A associação entre polidramnia e macrossomia fetal é amplamente descrita (Fisk et al., 1994), podendo causar complicações intraparto (distocia de ombro) e neonatais (hipoglicemia), entre outras.
 Figura 33.2 Polidramnia grave. Ressonância magnética – sagital T2 de feto com 27 semanas, portador de atresia
Figura 33.2 Polidramnia grave. Ressonância magnética – sagital T2 de feto com 27 semanas, portador de atresia
de esôfago. (Foto autorizada pelo Dr. Heron Werner.)
Figura 33.3 Incidência das malformações fetais nos casos de polidramnia (em porcentual). (Adaptada de Dashe
et al, 2002.)
A investigação sistemática das aneuploidias fetais nos casos de polidramnia isolada tem sido preconizada por alguns autores. Entretanto, Dashe et al. (2002), investigando o desfecho perinatal de 672 gestações com polidramnia, a partir do estudo de 93.332 casos, descreveram taxa de aneuploidias fetais de 10% nos fetos malformados. Dessa amostra, nos fetos sem anormalidades detectadas à ultrassonografia pré-natal (nível II) a taxa de aneuploidias foi de apenas 1%. Dessa maneira, vale considerar a indicação individualizada da investigação genética nos casos de polidramnia idiopática deva ser individualizada, contemplando os demais aspectos que cotejam o risco das pacientes para as aneuploidias fetais.
Aviram et al. (2015), investigando a polidramnia idiopática na gravidez com 34 semanas ou mais, referem sua associação com desfechos obstétricos e neonatais adversos – parto cesáreo, fase da dilatação prolongada, traçados da frequência cardíaca fetal anormais ou intermediários, descolamento prematuro da placenta (DPP), distocia de ombros e síndrome de angústia respiratória. O papel dos testes de avaliação da vitalidade fetal na polidramnia idiopática é incerto. Fisk et al. (1994) descreveram correlação inversa entre a pressão uterina na polidramnia e o pH do sangue de cordão do feto. À luz do conhecimento atual não é possível eleger nenhum dos testes disponíveis como de escolha no monitoramento pré-natal da polidramnia idiopática. Nos casos de polidramnia associados às patologias fetais ou maternas, a avaliação pré-natal da viabilidade fetal deve seguir os protocolos de condutas pertinentes a cada condição.
Tratamento
As intervenções terapêuticas nas causas primárias durante o período pré-natal, sejam maternas (controle glicêmico para as gestantes diabéticas), fetais (coagulação a laser das anastomoses arteriovenosas na síndrome de transfusão gêmeo-gemelar) ou placentárias (coagulação a laser de um corioangioma), devem diminuir o volume de LA, amenizando ou até mesmo revertendo o quadro em alguns casos. Na polidramnia idiopática ou naquelas condições em que não há terapêutica eficaz no período pré-natal podem ser usadas medidas paliativas (medicamentosas ou cirúrgicas) que visam apenas reduzir o volume de LA, independentemente da causa primária.
Entretanto, essas medidas só devem ser instituídas nos casos sintomáticos, nos quais se observam dispneia, metrossístoles ou hipertonia importante.
Amniodrenagem
A amniodrenagem precede em décadas a ultrassonografia. A técnica consistia na elevação da apresentação fetal com posterior inserção da agulha às cegas. Desde então, com o desenvolvimento da ultrassonografia, o monitoramento em tempo real aumentou significativamente a segurança do procedimento. Tradicionalmente, recomenda-se a drenagem de volume total de, no máximo, 2.000 ml. Tal recomendação visa reduzir o risco de complicações relacionadas com o procedimento, dentre elas a mais temida é o descolamento prematuro de placenta.
A técnica de amniodrenagem sob pressão negativa constante, ou amniodrenagem rápida, promove o esvaziamento de mais de 3,5L em menos de 30 min, com limite máximo de 5L por procedimento. Estudos recentes (Tabela 33.2) demonstraram que o risco de complicação dessa técnica varia de 0 a 15%. A complicação mais comum foi a RPM. A maior taxa de descolamento prematuro de placenta (14,81%) é descrita por Reisner et al. (1993). É provável que essa taxa esteja superestimada, pois o autor usou parâmetros histopatológicos na definição do diagnóstico, e não o evento clínico. Na maioria das vezes a amniodrenagem rápida é aceitável, desde que se respeite o limite de 5L, considerando o conforto que proporciona à paciente e a segurança aceitável do procedimento.
Indometacina
A descrição da associação entre o uso materno da indometacina, como tocolítico, e a diminuição do volume de LA data do final da década de 1980 (Kirshon et al., 1981; Moise et al., 1988). Desde então, esse fármaco vem sendo usado no tratamento da polidramnia (Moise, 1991); o mecanismo de ação é essencialmente a diminuição do débito urinário fetal (Kirshon et al., 1981). Os efeitos colaterais indesejáveis são a regurgitação tricúspide, a disfunção ventricular direita e o fechamento do ducto arterioso; este último, o mais temido, é dose-dependente, podendo ser observado a partir de 24 semanas. Na 27 a semana ocorre em 5% dos casos, chegando a 50% na 32 a semana de gestação (Dashe et al., 2002). A dose de indometacina geralmente usada no tratamento da polidramnia varia entre 1 e 3 g/dia (250 mg a 500 mg de 6/6 h), podendo chegar à dose máxima de 3 mg/kg/dia (Dashe et al., 2002). Iniciado o tratamento, é imprescindível o monitoramento pelo Doppler do ducto arterioso (DDA) (Figura 33.4).
Sulindac
É um inibidor das prostaglandinas que também pode ser usado no tratamento medicamentoso da polidramnia. Por se tratar de um fármaco que necessita de metabolização hepática para produzir o princípio ativo, é provável que o sulindac tenha menos efeitos colaterais no feto que a indometacina. Kramer et al. (1995) demonstraram que a concentração do metabólito ativo do sulindac é 50% menor no sangue fetal do que no materno. Räsänen e Jouppila (1995) randomizaram 20 pacientes em trabalho de parto prematuro comparando o sulindac com a indometacina, e observaram que o sulindac apresentou menor efeito constritivo no ducto arterioso quando comparado à indometacina (30% para o sulindac e 70% para a indometacina). O efeito no débito urinário fetal também é menor com o sulindac; consequentemente, o efeito terapêutico também é menos efetivo. A pouca experiência no manuseio desse fármaco sugere cautela e atenção às pesquisas em curso.
Tabela 33.2 Descrição das complicações mais frequentemente associadas com a técnica de amniodrenagem sob pressão negativa constante ou amniodrenagem rápida.
Conduta intraparto
O acompanhamento do trabalho de parto nas gestações com polidramnia, em especial nos casos mais graves, merece atenção especial. As condutas intraparto visam evitar, mas também conduzir, as complicações mais frequentes desse período. Optando pela via transpélvica, deve-se sempre avaliar, com generosidade, os benefícios da amniodrenagem ao início do trabalho de parto, que é imprescindível na maioria dos casos de polidramnia moderada e grave.
O obstetra no primeiro período deve estar atento à atividade uterina. Distinguem-se dois tipos de polidramnia, no que se refere à atividade uterina: um de baixa contratilidade e outro de alta contratilidade. Nos de baixa contratilidade, a hipertonia é leve ou está ausente, e a resposta à ocitocina é fisiológica. Na polidramnia de alta contratilidade, observam-se hipertonia e hipossistolia, a resposta à ocitocina é ineficiente e, consequentemente, o amadurecimento do corpo e do colo é laborioso. A redução do volume de LA atenua as anormalidades da dinâmica uterina.
A amniorrexe, espontânea ou artificial, também é extremamente delicada e deve ser bem conduzida. Na amniotomia, a criteriosa avaliação da altura da apresentação, a elevação das nádegas da paciente e a condução do escoamento do LA mantendo-se os dedos na vagina da paciente são aconselháveis. Desse modo, evitam-se casos de prolapso de cordão e apresentações anômalas.
O terceiro e o quarto período devem ser conduzidos com atenção especial; a sobredistensão uterina secundária à polidramnia predispõe às hemorragias pós-parto. A profilaxia com uterotônicos é imprescindível nesses casos.
Oligoidramnia
Em algumas décadas, a avaliação do LA e de seus determinantes evoluiu do mero interesse acadêmico da fisiologia feto-placentária para importante ferramenta de monitoramento intrauterino, especialmente nos casos de oligoidramnia. À luz dos conhecimentos atuais, o crescimento fetal restrito, o sofrimento fetal intraparto e a mortalidade perinatal estão associados com a oligoidramnia (ACOG, 1999). A indução do parto deve ser considerada em gestações a termo (Croom et al., 1992).
Figura 33.4 Descrição do acompanhamento fetal durante o uso de indometacina. DDA, dopplervelocimetria do ducto arterioso.
A prevalência de oligoidramnia na população de gestantes varia de 0,5 a 5,5%, de acordo com critérios usados para definição e com a população estudada. Tradicionalmente, a oligoidramnia foi definida como redução do volume de LA a valores inferiores a 300 ou 400m? (Goldstein, Filly, 1988). Atualmente, há tendência de se usar o volume de LA estimado pela ultrassonografia para essa definição. Assim, para que intervenções desnecessárias sejam evitadas e para que o desfecho obstétrico seja melhor, a definição de oligoidramnia deve ser a mais precisa possível. A oligoidramnia pode ser diagnosticada por meio de ultrassonografia, assim como a polidramnia, de maneira subjetiva ou semiquantitativa. Avaliação subjetiva depende essencialmente da experiência do observador, podendo haver dificuldade maior na comparação dos resultados. No entanto, quando se comparam examinadores experientes há boa correlação entre os dois métodos, com pequena variação interobservador (Philipson et al., 1983).
À ultrassonografia observa-se pequena quantidade de líquido entre as partes fetais e a parede uterina, com evidente diminuição do volume de líquido, o que prejudica a avaliação da morfologia fetal (Phelan et al., 1987) (Figura 33.5). Já os métodos semiquantitativos incluem o cálculo do ILA, ou a medida do MBV. Descrito por Phelan et al. (1987), o ILA é calculado após a divisão do útero em quatro quadrantes no nível da cicatriz umbilical e com a medida do maior bolsão vertical encontrado em cada um deles, livre de partes fetais e de cordão umbilical. O somatório dessas medidas consiste no ILA. A técnica do maior bolsão vertical, por sua vez, consiste na medida
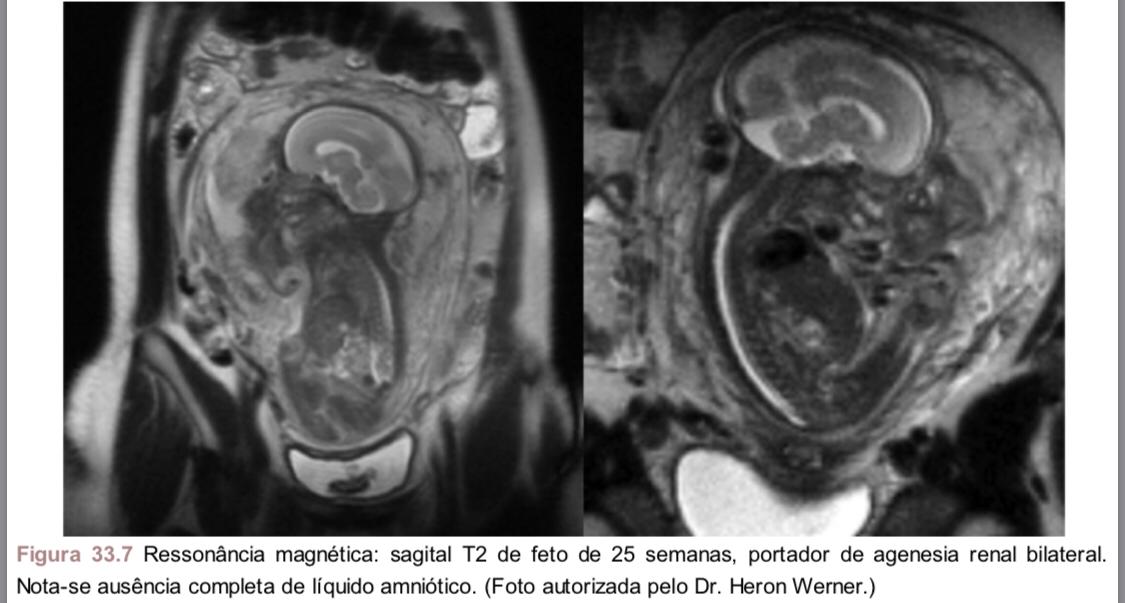
do diâmetro vertical do maior bolsão de LA também livre de partes fetais e de cordão umbilical. A definição mais aceita de oligoidrâmnio é o MBV < 2 cm (Figura 33.6). Mais recentemente, o arsenal diagnóstico na propedêutica fetal foi enriquecido com outros métodos de imagem. A RM tem sido usada, essencialmente, para elucidar as malformações fetais, bem como para sobrepor as dificuldades de pormenores ultrassonográficos oriundos da diminuição acentuada de LA (ausência de janela acústica). O volume de LA é mais bem visualizado e quantificado pela RM, facilitando o diagnóstico da oligoidramnia (Figura 33.7). A quantidade de LA previamente aferido por RM foi comparada ao MBV e ao ILA obtidos pela ultrassonografia. O volume total do LA foi medido diretamente na cesariana (Hombo et al., 2002). A RM mostrou maior correlação estatística com o volume de líquido medido no parto, mas os três métodos foram estatisticamente comparáveis na predição de oligoidramnia.
Figura 33.5 Adramnia: não visualização de líquido amniótico entre as partes fetais, o cordão umbilical e a placenta.
Figura 33.6 Avaliação semiquantitativa do volume do líquido amniótico. Maior bolsão vertical menor que 2 cm.
Etiologia
Há suspeita clínica quando a paciente relata perda de líquido, no caso da ruptura das membranas ovulares, ou quando no exame físico o fundo de útero for menor que o esperado para a idade gestacional e a percepção das partes fetais for evidente. Os principais grupos de causas de oligoidramnia incluem a RPM, a insuficiência placentária, o pós-datismo e as malformações fetais, com destaque para as malformações do aparelho urinário (Tabela 33.3). No caso de RPM, a idade gestacional é crucial para se determinar da conduta a ser seguida. Devem ser avaliados os riscos da prematuridade, quando for essa a questão, e os riscos maternos e fetais da conduta expectante, com destaque à infecção, para ambos, e a hipoplasia pulmonar, nos prematuros extremos.
Figura 33.7 Ressonância magnética: sagital T2 de feto de 25 semanas, portador de agenesia renal bilateral. Nota-se ausência completa de líquido amniótico. (Foto autorizada pelo Dr. Heron Werner.)
A insuficiência placentária pode ser manifestação de doença primária da placenta ou secundária à doença de base materna como hipertensão arterial, diabetes, doença renal crônica, doenças autoimunes como lúpus eritematoso sistêmico, entre outras. Nesses casos, a oligoidramnia está associada ao crescimento fetal restrito, e seria mais um marcador de sofrimento fetal crônico. Dentre as condições fetais, as gestações gemelares estão entre as principais causas de insuficiência placentária e oligoidramnia. Nas gestações gemelares monocoriônicas, a oligoidramnia também pode ser causada por síndrome de transfusão gêmelo-gemelar (STGG), na qual o outro gemelar cursará com polidramnia.
Tabela 33.3 Condições associadas com a oligoidramnia.
Fetais
Anomalias cromossômicas
Anomalias congênitas
Restrição de crescimento
Pós-datismo
Ruptura de membranas ovulares
Placentárias
Descolamento prematuro da placenta
Transfusãofeto-fetal
Maternas
Insuficiência placentária
Hipertensão
Pré-eclâmpsia
Diabetes melito
Fármacos
Inibidores da síntese de prostaglandinas
Inibidores da enzima conversora da angiotensina
Idiopática
AdaptadadePeipert &Donnenfeld,1991.
A gestação prolongada é outra importante causa de oligoidramnia por insuficiência placentária, quando também se discute a importância da oligoidramnia como marcador de sofrimento fetal. Já em relação às malformações associadas à oligoidramnia, destacam-se as do aparelho urinário fetal que impedem a eliminação adequada da urina, como a agenesia renal bilateral, a doença renal policística e as obstruções urinárias baixas bilaterais (Figura 33.8). O acometimento fetal nesses casos é precoce, com a oligoidramnia muitas vezes se manifestando desde o início do 2o. trimestre de gestação. Kemper & Mueller-Wiefel (2007) e Bunchman (2000) publicaram revisão sobre o prognóstico dos fetos com oligoidramnia de origem renal, diagnosticados no período pré-natal. Os autores salientaram que, embora muito se tenha avançado no tratamento dessas crianças, com as derivações vesicoamnióticas e com o maior cuidado intensivo ao nascimento, ainda são patologias graves, com alta mortalidade, especialmente por hipoplasia pulmonar. Entretanto, já existem algumas alternativas para o tratamento da função renal desses recém-nascidos ou crianças, como a diálise e o transplante, de modo que a doença renal, do ponto de vista técnico, não pode mais ser considerada fator
limitante da sobrevida. Os resultados obtidos por alguns pesquisadores com a diálise são encorajadores, possibilitando crescimento e qualidade de vida aceitáveis (Ledermann et al., 2000; Shroff & Ledermann, 2009; Peipert & Donnenfeld, 1991).
Figura 33.8 Ressonância magnética – sagital T2 de feto com 26 semanas, portador de válvula de uretra posterior. Nota-se oligoidramnia acentuada. (Foto autorizada pelo Dr. Heron Werner.)
Alguns fármacos, como os inibidores da enzima conversora da angiotensina e os inibidores da síntese de prostaglandinas, também estão associados a oligoidrâmnio. Outras vezes, nenhuma causa descrita é encontrada, e a paciente é classificada como tendo oligoidramnia idiopática (Rotschild et al., 1990). Independentemente da causa, a oligoidramnia é responsável por algumas repercussões desfavoráveis para o feto. Está associada, como descrito, com o sofrimento fetal e a hipoplasia pulmonar. De modo geral, a hipoplasia pulmonar é uma complicação da oligoidramnia de início precoce. Quanto menor a idade gestacional acompanhada de oligoidramnia, maiores a incidência e a mortalidade oriunda da hipoplasia pulmonar. Normalmente, a hipoplasia pulmonar está condicionada às malformações obstrutivas do trato urinário ou à ruptura prematura das membranas pré-termo. A hipoplasia pulmonar em função da ruptura prematura das membranas pré-termo foi encontrada em 50% dos casos nas gestações com 19 semanas, e em 10% nas gestações com 25 semanas (uma média de 16% antes das 29 semanas). Nas gestações com mais de 31 semanas, a incidência foi de 1%, segundo Rotschild et al.; outros autores tiveram resultados semelhantes (Kilbride et al., 1996; Lauria et al., 1995). Três possibilidades tentam explicar a hipoplasia pulmonar. Primeiro, a compressão torácica poderia impedir a sua expansão e a do pulmão. Em segundo lugar, a falta dos movimentos respiratórios fetais diminuiria a expansão pulmonar; e o terceiro, modelo mais aceito, envolve uma falha na retenção de líquido, sendo prejudicial ao crescimento e desenvolvimento do pulmão (Askenasi Perlman, 1979). Os pulmões não são simplesmente pequenos, mas estruturalmente imaturos, com menor quantidade de canais aéreos e alvéolos (Hofmeyr, 1999).
Outros achados clínicos no recém-nascido de gestação com oligoidramnia grave e precoce incluem a sequência de Potter, com deformidades no polo cefálico, na face e nas extremidades. A oligoidramnia também pode ser responsável por apresentações fetais anômalas, compressão do cordão umbilical, pós-maturidade, líquido meconial e aumento da incidência de cesarianas (Defoort, 2005).
Tratamento
O tratamento depende, essencialmente, da causa e da idade gestacional do acometimento. É necessária investigação cuidadosa na busca da causa para a oligoidramnia. Devem-se fazer anamnese e exame físico cuidadosos, procurando sinais e sintomas de amniorrexe, uso de medicações e fatores de risco para insuficiência placentária e CIR. Em seguida, a ultrassonografia com o intuito de identificar malformações fetais deve ser realizada, com especial atenção ao diagnóstico de malformações do sistema urinário. Em casos de insuficiência placentária e CIR, a biometria intrauterina é menor que a esperada e a dopplervelocimetria da artéria umbilical
pode estar alterada, o que geralmente não acontece em casos de malformações fetais. À semelhança da polidramnia, as indicações para a investigação do cariótipo fetal devem contemplar cada caso de modo mais abrangente.
À exceção dos casos associados a malformações fetais, o prognóstico fetal está intimamente relacionado com sua vitalidade, sendo imprescindível seu controle rigoroso, com os métodos disponíveis, como a cardiotocografia, a ultrassonografia e o Doppler, estando o parto indicado nos casos em que o bem-estar fetal não pode ser assegurado.
Hidratação materna
Os estudos sobre o efeito da hidratação materna no volume de LA têm resultados conflitantes. A infusão venosa de fluidos parece aumentar o volume de LA (Deka & Malhotra, 2001), o que pode ser interessante quando a conduta expectante for uma opção. Deka & Malhotra (2001) avaliaram o efeito da hidratação oral materna com 2? de água em 1 h no volume de LA medido pelo ILA. A média foi de 6,99 cm para 10,48 cm, o que foi estatisticamente significativo. Dois grupos (Umber & Chohan, 2007; Strong et al., 1990) também conseguiram mostrar aumento significativo do volume de LA com a hidratação venosa, sugerindo que a hidratação poderia auxiliar no manejo da oligoidramnia. O benefício da hidratação materna também depende da causa básica de oligoidramnia. Casos decorrentes de malformações fetais provavelmente não irão se beneficiar dessa terapêutica.
Amnioinfusão
A amnioinfusão é o procedimento no qual é infundido soro fisiológico na cavidade amniótica por meio da amniocentese. A infusão de 250 ml de solução salina aumenta o ILA em 4 cm (Hofmeyr et al., 1996), podendo ser realizada para diagnóstico, para melhorar a visualização das estruturas fetais à ultrassonografia, ou com o propósito terapêutico, na tentativa de diminuir a incidência de hipoplasia pulmonar ou de sofrimento fetal intraparto (ACOG, 1991). No caso do uso intraparto, a amnioinfusão não se mostrou eficaz na prevenção de síndrome de aspiração meconial (Hofmeyr apud Enkin et al., 1995); no entanto, metanálise com nove estudos randomizados mostrou que a amnioinfusão diminuiu a incidência de cardiotocografia com padrão desfavorável, de parto operatório e de pH baixo no cordão umbilical (Chhabra et al., 2007). Estudo posterior realizado por Chhabra et al. também constatou melhora dos desfechos descritos anteriormente em pacientes submetidas à amnioinfusão, que não é um procedimento isento de riscos. Uma revisão de 186 departamentos acadêmicos nos EUA, com 22 mil amnioinfusões por ano, mostrou aumento do risco de hipertonia uterina, alteração do ritmo cardíaco fetal, amnionite, ruptura uterina e insuficiência respiratória ou cardíaca materna.
Fonte: Montenegro, Carlos Antonio Barbosa Rezende obstetrícia / Carlos Antonio Barbosa Montenegro, Jorge de Rezende Filho. – 13. ed. – Rio de Janeiro : Guanabara Koogan, 2017.